Как мы видели, в рамках классической физики планетарная модель атома противоречит опыту. Это указывало на то, что законы классической физики неприменимы в масштабах атома.
Первую попытку «угадать» новые законы атомной физики предпринял молодой датский физик Нильс Бор в 1913 году.
В стремлении «спасти» планетарную модель атома он дополнил ее положениями, которые получили впоследствии название «постулатов Бора».
Вот эти постулаты:
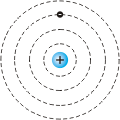
1.Электроны в атомах движутся только по определенным орбитам, называемым стационарными (рис. 26.5). Каждой орбите соответствует определенная энергия электрона 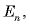 где
где 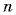 - номер орбиты.
- номер орбиты.
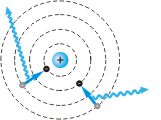
2.Электроны излучают фотоны только при переходе с одной орбиты на другую, с меньшей энергией. Энергия излученного фотона равна разности энергий электрона на орбитах: 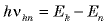 (рис. 26.6). Отсюда следует, что атом может излучать свет только с частотами
(рис. 26.6). Отсюда следует, что атом может излучать свет только с частотами 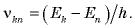
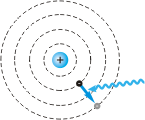
Атом может также поглощать фотоны. При поглощении фотона электрон в атоме переходит со стационарной орбиты с меньшей энергией на орбиту с большей энергией. Следовательно, каждый атом может поглощать свет только с частотами 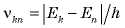 (рис. 26.7).
(рис. 26.7).
Состояние атома, в котором все электроны находятся на стационарных орбитах с наименьшей возможной энергией, называется основным. Все другие состояния атома называются возбужденными.