- Все вещества состоят из мельчайших частиц, которые находятся в непрестанном хаотическом движении и взаимодействуют друг с другом.
- Величины, характеризующие свойства отдельных молекул вещества, называют микроскопическими параметрами, а характеризующие состояние макроскопических тел в целом, называют макроскопическими параметрами.
- Уравнением состояния называется соотношение между макроскопическими параметрами (температурой, объемом и давлением). Основная задача молекулярно-кинетической теории — найти уравнение состояния вещества, установив связь между макроскопическими и микроскопическими параметрами.
- Относительная молекулярная масса
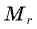 равна отношению массы
равна отношению массы 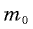 молекулы данного вещества к 1/12 массы атома углерода
молекулы данного вещества к 1/12 массы атома углерода 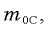 то есть
то есть 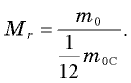
- Один моль — это количество вещества, которое содержит столько же молекул, сколько атомов углерода содержится в 12 г углерода. Массу вещества, взятого в количестве одного моля, называют молярной массой. Постоянной Авогадро называется число молекул в одном моле:
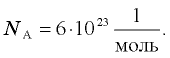
- Температура характеризует состояние теплового равновесия: тела, находящиеся в тепловом равновесии, имеют одинаковую температуру.
- Абсолютной температурой называется температура по шкале Кельвина, а нуль по этой шкале — абсолютным нулем температуры. Он соответствует
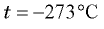 по шкале Цельсия.
по шкале Цельсия. - Изопроцессы: для данной массы газа
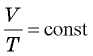 при
при 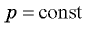 (изобарный процесс);
(изобарный процесс); 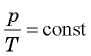 при
при 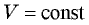 (изохорный процесс);
(изохорный процесс); 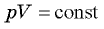 при
при 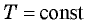 (изотермический процесс).
(изотермический процесс). - Уравнение Клапейрона: для данной массы газа произведение давления газа на его объем, деленное на абсолютную температуру газа, есть величина постоянная:
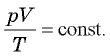
- Закон Авогадро: при одинаковых температуре и давлении в равных объемах различных газов содержится одинаковое число молекул. Следствием закона Авогадро является соотношение
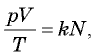 где
где 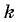 — постоянная Больцмана.
— постоянная Больцмана. - Уравнение Менделеева—Клапейрона:
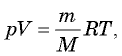 где
где 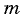 — масса газа,
— масса газа, 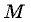 — его молярная масса. Универсальная газовая постоянная
— его молярная масса. Универсальная газовая постоянная 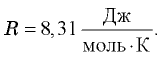
- Идеальным газом называется модель реального газа, в которой пренебрегают размерами молекул газа и их взаимодействием между столкновениями.
- Основное уравнение молекулярно-кинетической теории:
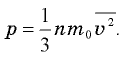
- Средняя кинетическая энергия молекул
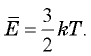 Поэтому температура является мерой средней кинетической энергии движения молекул.
Поэтому температура является мерой средней кинетической энергии движения молекул. - В кристаллах атомы или молекулы расположены упорядоченно, образуя кристаллическую решетку; кристаллы плавятся при определенной температуре, называемой температурой плавления.
- В аморфных телах есть только «ближний порядок» в расположении атомов и молекул; аморфные тела обладают текучестью; аморфные тела не имеют определенной температуры плавления.
- В расположении молекул в жидкости существует только ближний порядок.
Главное в главе 5. Молекулярная физика
Молекулярная физика и термодинамика. 2014
